「控糖」促腫瘤轉移?葡萄糖限制誘導肺部促轉移免疫環境新機制
整體情況及亮點介紹
2025年7月15日,中山大學鄺棟明教授、魏瑗副教授團隊在《Cell》期刊發表題為《Glucose Restriction Shapes Pre-Metastatic Innate Immune Landscapes in Lung through Exosomal TRAIL》(影響因數:42.5)的研究論文。該研究通過大規模臨床數據、多組學分析與體內實驗,首次揭示葡萄糖剝奪可通過外泌體TRAIL重塑肺部免疫環境,誘導轉移前生態位形成的機制,並提出相應的干預策略。本研究由中山大學、中山大學香港高等研究院等單位合作完成。
背景、研究初衷、研究過程、初步成果/驗證
葡萄糖代謝是支撐腫瘤快速增殖的核心能量來源。近年來,抑制糖代謝(如低碳水化合物飲食)逐漸成為一種被廣泛關注的潛在抗腫瘤策略。然而,在腫瘤治療中,僅控制腫瘤生長並不能有效改善患者預後,遠處轉移才是導致高死亡率的根本原因。
葡萄糖剝奪對細胞而言是一種重要的代謝應激。一個關鍵問題是:在限制葡萄糖代謝的過程中,是否可能誘導腫瘤細胞向更具侵襲性的表型演化? 近年來研究提示,靶向葡萄糖代謝不僅影響腫瘤能量供給,也可能啟動多種應激反應,改變腫瘤微環境組成,特別是影響免疫調控機制。然而,目前尚缺乏系統研究探討糖代謝干預對遠端免疫環境和轉移前生態位形成的影響。
葡萄糖代謝缺陷與轉移風險升高相關
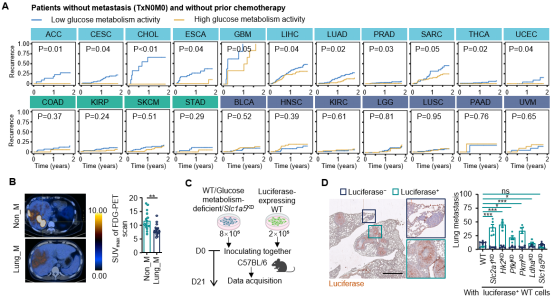
研究首先分析了15種腫瘤類型的大規模患者數據,發現葡萄糖代謝活性較低的患者術後兩年內復發風險顯著升高。在肝癌患者中,術後發生肺轉移者的腫瘤組織葡萄糖代謝顯著低於未轉移者。
在多種小鼠腫瘤模型中,研究者進一步證實,無論是通過低碳水化合物飲食還是遺傳干預降低腫瘤糖代謝水準,均顯著增強肺轉移傾向。需要強調的是,轉移增加並非由於葡萄糖剝奪增強了腫瘤細胞自身的遷移能力,而是葡萄糖代謝缺陷的細胞通過「旁觀者效應」促進鄰近代謝正常腫瘤細胞的轉移能力。
機制揭示:TRAIL介導的免疫耗竭促進轉移前生態位形成
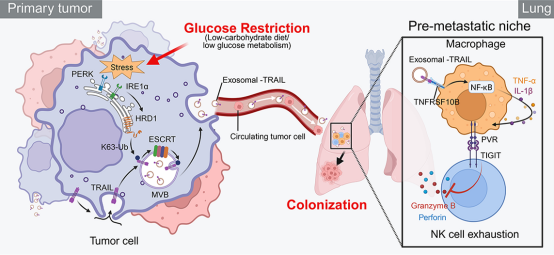
機制研究顯示,葡萄糖剝奪誘導腫瘤細胞內質網應激,啟動E3泛素連接酶HRD1,促進TRAIL在K63位點的泛素化修飾,並通過ESCRT複合體將其包裝入外泌體。該類外泌體攜帶的TRAIL釋放至肺部後,可誘導PVR⁺巨噬細胞極化,進而通過PVR–TIGIT軸耗竭肺部NK細胞功能,從而建立有利於腫瘤定植的免疫微環境。
在多個動物模型中,阻斷TIGIT可顯著降低肺部轉移負擔,且對原位腫瘤生長亦有抑制作用,提示TIGIT可能成為代謝應激相關轉移的干預靶點。
研究難點
該研究歷時約7 年。研究初期,團隊在多種癌種中觀察到一個令人意外的現象:糖代謝活性較低的腫瘤竟然與術後復發密切相關,這一顛覆認知的結果令人難以置信。為驗證這一發現,研究者系統整合了臨床樣本與病理資訊,並通過RNA 測序、乳酸脫氫酶(LDH)活性檢測、空間轉錄組分析以及 PET-CT 成像等多維度手段開展驗證性研究,結果一致顯示:發生肺轉移的肝癌患者,其原發腫瘤組織中的葡萄糖代謝水準顯著低於未轉移者。進一步的小鼠實驗亦表明,低碳水化合物飲食在抑制原位腫瘤生長的同時,反而增強了遠處肺轉移的發生。
這一現象令人困惑:傳統觀點認為糖代謝的活躍為腫瘤生長和擴散提供能量支持,而實驗結果卻顯示,在糖代謝受到抑制的背景下,腫瘤轉移反而增加。這一結果不僅具有理論上的悖論性,也挑戰了「靶向糖代謝可抑制腫瘤進展」的既有框架。儘管面臨重重疑問,研究團隊始終認為這一反常現象背後潛藏著值得深入挖掘的重要機制。
經過研究者的大量文獻調研、細緻觀察與反復思考,研究者逐漸意識到,腫瘤組織內部代謝異質性普遍存在,高糖代謝與低糖代謝區域往往並存。這一發現提示我們應摒棄將腫瘤視為代謝同質體的觀念,轉而關注腫瘤內不同成分之間的功能協同互作。由此,研究團隊提出假設:葡萄糖代謝受限的腫瘤細胞可能並非直接具備更強的轉移能力,而是通過「旁觀者效應」影響其鄰近的正常代謝腫瘤細胞,從而間接促進轉移。
圍繞該假說,團隊設計並巧妙的體內轉移模型,經過反復驗證,最終證實葡萄糖低的腫瘤細胞可通過外泌體-免疫軸重塑遠端免疫環境、促進代謝正常的細胞發生肺轉移。這一發現不僅深化了我們對代謝–免疫–轉移之間的因果鏈條的理解,也為腫瘤代謝靶向治療策略的優化提供了理論依據與實驗支持。
研究意義、應用前景
該研究從臨床現象出發,結合多組學與體內實驗證據,系統揭示了葡萄糖限制可通過外泌體-免疫軸重塑遠端免疫環境、促進轉移的機制,並提出TIGIT通路作為聯合干預靶點,具有重要的基礎研究價值和臨床轉化潛力。
該研究結果提示,在腫瘤治療或預防中,應謹慎評估代謝干預的系統性影響。對於腫瘤患者而言,過度「控糖」可能帶來轉移風險;對於尚未確診但存在潛在病灶的個體而言,極端的低碳水飲食亦可能為腫瘤轉移創造條件。
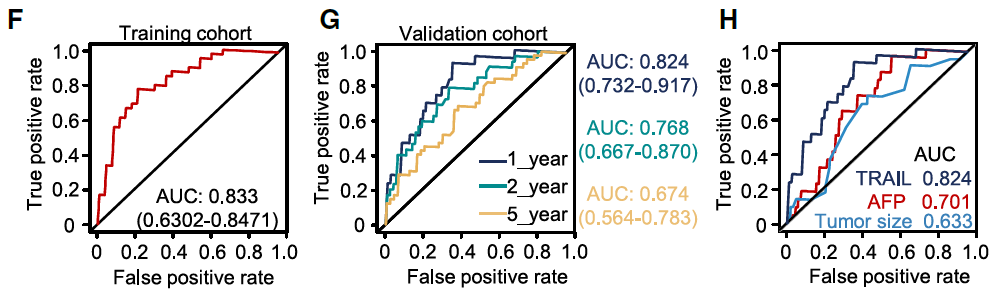
在臨床轉化方面,團隊發現血漿中外泌體TRAIL水準在預測肝癌術後肺轉移風險方面表現出色,優於傳統標誌物AFP及腫瘤體積,未來有望作為早期分層管理工具。