J Clin Invest丨貝錦新團隊揭示超級增強子驅動宮頸癌惡性進展的新機制
宮頸癌(Cervical cancer)作為全球女性第四大常見惡性腫瘤,其發病率和死亡率居高不下,嚴重威脅女性健康。宮頸癌發生發展涉及多種因素,包括高危型HPV亞型感染、個體的遺傳易感性及環境因素等。儘管早期患者可以通過手術和放化療獲得良好預後,但晚期或轉移性患者預後較差,5年生存率僅有16.5%。因此,深入研究驅動宮頸癌發生發展的致癌機制,探索新型診療靶點和診療策略,是提高宮頸癌患者療效的迫切需求,對於降低疾病負擔具有重要意義。
超級增強子(Super-enhancer, SE)作為高階染色質調控元件,通過協同多個增強子區域聚集而成,能夠驅動腫瘤關鍵基因的異常表達。既往研究雖提示SE在宮頸癌等多種癌症發生中的作用,但受限於技術手段和臨床樣本來源,目前大多數篩選SE的研究多依賴於體外傳代細胞系,難以真實反映腫瘤組織內SE的生物學特性。因此,解析宮頸癌腫瘤組織特異SE圖譜及其調控網路,對揭示腫瘤表觀遺傳驅動機制具有重要科學價值,有助於瞭解宮頸癌的致病機制,發現表觀遺傳治療靶點和策略,最終提高患者預後。
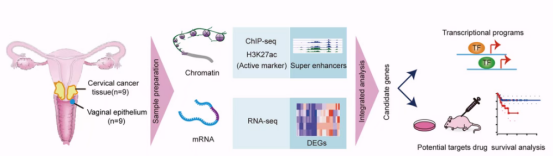
中山大學腫瘤防治中心研究員、中山大學香港高等研究院院長助理貝錦新團隊在Journal of Clinical Investigation發表題為Super-Enhancer-Driven EFNA1 Fuels Tumor Progression in Cervical Cancer via the FOSL2-Src/AKT/STAT3 Axis的研究論文。該研究通過整合染色質免疫沉澱測序(ChIP-Seq)和轉錄組測序(RNA-Seq)數據,描繪了宮頸癌特異的SE圖譜,進一步結合體內、體外模型和分子機制研究,揭示了腫瘤特異的EFNA1-SE通過驅動EFNA1表達促進宮頸癌惡性進展的機制,並探討了靶向EFNA1下游信號通路治療宮頸癌的臨床應用前景。

該研究通過整合9對宮頸癌腫瘤組織及對照組織的ChIP-Seq(H3K27ac)和RNA-Seq多組學數據,首次在組織水準構建了宮頸癌組織特異性SE全景圖譜,鑒定了腫瘤中啟動的SE相關基因集(圖1)。通過TCGA生存分析鎖定關鍵SE驅動基因EFNA1,其高表達與患者不良預後顯著相關(HR=2,P=0.0047),提示了SE驅動的EFNA1在宮頸癌進展中起關鍵作用。
該研究運用CRISPR/Cas 9技術特異性敲除基因組EFNA1-SE的核心增強子元件(E1和E2),發現其缺失可顯著降低EFNA1的轉錄水準(mRNA分別下降 51%和63%)。雙螢光素酶報告實驗顯示,將E1或E2構建至EFNA1啟動子前面可以顯著促進EFNA1的轉錄活性,而使用SE相關BRD4抑制劑JQ-1處理則顯著逆轉其促進作用。機制研究表明,EFNA1-SE可以招募乙醯化組蛋白H3K27ac以及FOSL2;FOSL2作為關鍵轉錄因數結合到SE區域,協同H3K27ac修飾共同啟動EFNA1表達。功能學實驗證實,EFNA1-SE缺失或者EFNA1沉默可顯著抑制宮頸癌的增殖、遷移、侵襲及體內成瘤能力,而過表達EFNA1則顯著促進這些能力。這些結果說明EFNA1-SE及其調控的EFNA1影響宮頸癌的惡性進展。
為了深入探究EFNA1在宮頸癌中的促癌機制,該研究聯合利用RNA-seq、蛋白晶片和Co-IP實驗,發現EFNA1以順式作用(cis-regulation)方式結合EphA2受體FNⅢ結構域,通過抑制EphA2磷酸化水準並促進其蛋白降解,進而啟動下游Src/Akt/STAT3信號軸,促進宮頸癌的惡性進展。值得注意的是,靶向抑制該通路的關鍵節點(如Saracatinib抑制Src、MK2206抑制Akt或者Stattic 抑制STAT3)可有效逆轉EFNA1過表達所引發的促癌效應。

綜上,該研究揭示了宮頸癌組織特異的SE調控網路,並鑒定EFNA1作為SE驅動的新型致癌因數,進一步揭示了EFNA1-EphA2-Src/AKT/STAT3信號軸的級聯啟動機制及其在宮頸癌中的促癌作用(圖2)。該研究不僅深化了對宮頸癌表觀遺傳調控機制的理解,更為開發SE及其下游調控網路靶向療法及聯合用藥策略提供了理論依據。
中山大學腫瘤防治中心劉樹強博士後、程茜茜博士生、何帥副研究員為該論文共同第一作者;中山大學腫瘤防治中心貝錦新研究員、羅春玲副研究員和藍春燕教授為該論文的共同通訊作者。
原文鏈接:https://www.jci.org/articles/view/177599
貝錦新課題組主要從事精准醫學和轉化醫學研究,針對腫瘤臨床表徵異質性,利用個體和單細胞水準的基因組、表達譜等多層次、多組學資訊,挖掘與腫瘤發生發展及其異質性相關的分子、細胞及其作用網路,研究候選分子、細胞調控腫瘤進展的重要機制,發現與腫瘤早期精准診斷相關的分子標誌物,篩選針對腫瘤微環境演進關鍵事件的精准診治靶標,為實現腫瘤的個體化防診治提供有效解決方案。至今發表SCI論文110餘篇,其中包括國際頂級專業雜誌Cell、Lancet Oncology、Nature Genetics、Journal of Clinical Investigations,Nature Communications 等。課題組長期招聘各類科研人員,歡迎對相關領域感興趣的博士後,博士生加入。

